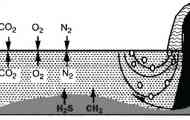
Јаглерод диоксид во карбонат систем

Без сомнение дека CO2 постои во секоја природна вода во поголема или помалку концентрација. Јаглерод диоксид има многу добра растворливост, што е ограничено на размена со атмосфера. Растворен копродукции2 оди во коалиска киселина (H2Ко3) во помало количество (приближно 0,1-0,2%).
Ко2+ Час2O => Час2Ко3.
Дури и ако овој процес е изразен слабо, формирањето на киселина неизбежно води до намалување на pH вредноста. Водата збогатена со јаглен киселина може да достигне pH вредности околу 5, а понекогаш има пониски. Кога се раствора јаглерод диоксид во вода, се зголемува спроводливоста. Ова се должи на формирањето на јони:
Час2Ко3+ Час2O => Час3О+ + HCO3-,
Се појавуваат хидроксониум и хидроцеробонат јонски јон. Баргабонат јон влегува во соединенија со алкални земни метали, од кои е најважен е CA (HCO3)2 (сол на коалиска киселина) и постои во вода целосно дисоцијација, т.Е. во форма на катјони и анјони.

Односот на јаглерод диоксид и анјони на коалиска киселина во вода во зависност од pH (криви за море и свежа вода)
Калциум бикарбонат е добро растворлив во вода. Оваа врска е формира привремена ригидност. Бикарбонат содржи хемиски поврзан СО2, кој се нарекува во согласност со оваа "поврзана коалиска киселина". Износот на калциум бикарбонат во воден раствор не се менува ако има дополнителен CO2, или рамнотежа ко2, Слободен јаглерод диоксид.
Ако истата количина на бесплатни CO2, Како CA (HCO3)2 Достапно, тогаш водата е во т.н. калциум рамнотежа - коалиска киселина. Често водата во која е растворена бесплатно2, Што е потребно за одржување на рамнотежата "калциум - јаглен киселина". Решението во овој случај се нарекува "слободна оласаризирана киселина". Оваа коалиска киселина е хемиски активна, но реакцијата бара соодветните соединенија.
Така, на пример, варовник се раствора (caco3), како што е тоа што содржината на калциум бикарбонат се зголемува повторно, а водата има тенденција на рамнотежа калциум - коалинска киселина. Слободен вишок коалиска киселина ги раствора пасивните слоеви во метални цевководи, исто така ги уништува цевките од бакар и водство, како резултат на тоа, од една страна, водоотпорни комуникации се оштетени, од друга страна, водата може да се збогати со токсични соединенија на метали. Ако водата не е доволно висока концентрација на слободен јаглероден диоксид, калциум карбонат паѓа во седиментот (CACO3). Тоа е познато за нас како варовник кој е практично нерастворлив во вода.
Трансформациите помеѓу бикарбонат и калциум карбонат се изразени со следната равенка:
Ко2 Нејас (Десна стрелка)
Ca (hco3)2 <=> CACO3+ Ко2+ Час2О
Ко2 вишок (Лева стрелка)
Јасно е дека транзицијата од еден вид на комуникација со друг е секогаш придружена со промени во pH вредноста, ако со недостаток на CO2 варовник паѓа, тогаш pH вредноста треба да се зголеми. И обратно, во вишок ко2 PH вредноста се намалува. Различни видови на ко-врски2, Со што се запознавме овде, како:
Јаглерод диоксид = ко2;
Коалиска киселина = h2Ко3;
Хидроцеробонат = HCO3-, почесто како CA (HCO3)2 и исто така се нарекува бикарбонат;
Карбонат = копродукции32-, Најчесто во форма на CACO3
Овие форми делумно можат да постојат во комбинација во вода. Вредноста на pH зависи, која е преовладува. Во мека кисела вода со pH 6, околу 80% јаглероден диоксид ќе бидат присутни во форма на CO2 или во форма на коалиска киселина и само околу 20% во форма на јаглеводобордни.
На pH 7, соодносот станува друг - преовладува HCO3. На pH 8-9 hCO3- е над 90%, и HCO3 и карбонати, како што е CACO3 негативен. Во морска вода има сосема различни модели. Границата помеѓу јаглеродниот диоксид и бикарбонат е само малку измешана лево, но значително посилна промена е забележана помеѓу бикарбонат и карбонат. Ова води кон фактот дека pH-регионот е оптимален за аквариуми со морска вода (pH 8-8.5), практично нема бесплатна карбонска киселина, но постои голема количина на карбонати.
Тоа е особено важно за морските животни работи. Картирање на организми, пред се корални, се наоѓаат во морето оптимални услови (доволен вар). Особено, површинската вода што се меша со атмосферата е одложена со калциум карбонат, а поголема од поголемата температура на водата. Постудена вода, толку повеќе може да апсорбира CO2. Затоа, дијатомските организми на ладни мори формираат силицинска киселина тело. Растворливост копродукции2 Исто така, се зголемува со зголемена длабочина, како резултат на ова, количината на карбонати се намалува во водата, па коралните гребени се толку популарни за аквариуми само во топлата површински води на тропските предели.
![Аквариум и обратен осмоза систем]() Аквариум и обратен осмоза систем
Аквариум и обратен осмоза систем![Активиран јаглерод за аквариум - да или не.]() Активиран јаглерод за аквариум - да или не.
Активиран јаглерод за аквариум - да или не.![Параметри на вода во аквариум - ph, нитрати, фосфор]() Параметри на вода во аквариум - ph, нитрати, фосфор
Параметри на вода во аквариум - ph, нитрати, фосфор![Ph во аквариум: слика, видео, опис, преглед.]() Ph во аквариум: слика, видео, опис, преглед.
Ph во аквариум: слика, видео, опис, преглед.![Киселини, бази и соли]() Киселини, бази и соли
Киселини, бази и соли![Зошто растенијата на тенкиум умираат?]() Зошто растенијата на тенкиум умираат?
Зошто растенијата на тенкиум умираат?![Методи на растечки аквариумски растенија]() Методи на растечки аквариумски растенија
Методи на растечки аквариумски растенија![Каква улога и вредности аквариумски растенија во аквариумот....]() Каква улога и вредности аквариумски растенија во аквариумот....
Каква улога и вредности аквариумски растенија во аквариумот....![Вода ригидност во аквариумот: како да се зголеми и како да се намали...]() Вода ригидност во аквариумот: како да се зголеми и како да се намали...
Вода ригидност во аквариумот: како да се зголеми и како да се намали...![Растворен во вода гасови]() Растворен во вода гасови
Растворен во вода гасови![Опрема за морски аквариум]() Опрема за морски аквариум
Опрема за морски аквариум![Kabomba: видови, опис, одгледување, содржина]() Kabomba: видови, опис, одгледување, содржина
Kabomba: видови, опис, одгледување, содржина![26 Аквариумски растенија кои имаат потреба од мала светлина...]() 26 Аквариумски растенија кои имаат потреба од мала светлина...
26 Аквариумски растенија кои имаат потреба од мала светлина...![Сите за дрво во аквариум]() Сите за дрво во аквариум
Сите за дрво во аквариум![Карактеристики на содржината на жителите на аквариумот...]() Карактеристики на содржината на жителите на аквариумот...
Карактеристики на содржината на жителите на аквариумот...![Круз: опис, ставови, фотографии]() Круз: опис, ставови, фотографии
Круз: опис, ставови, фотографии![Репродукција на аквариум растенија]() Репродукција на аквариум растенија
Репродукција на аквариум растенија![Оксидатор во аквариум: што е тоа и како функционира, направете го тоа сами...]() Оксидатор во аквариум: што е тоа и како функционира, направете го тоа сами...
Оксидатор во аквариум: што е тоа и како функционира, направете го тоа сами...![Ryukin риба: содржина, одгледување, опис]() Ryukin риба: содржина, одгледување, опис
Ryukin риба: содржина, одгледување, опис![Salvia sached содржина опис фото за репродукција.]() Salvia sached содржина опис фото за репродукција.
Salvia sached содржина опис фото за репродукција.![Eukhorenia lazzore или вода, еухроренија одлична или вода хиацинт, eukhorenny....]() Eukhorenia lazzore или вода, еухроренија одлична или вода хиацинт, eukhorenny....
Eukhorenia lazzore или вода, еухроренија одлична или вода хиацинт, eukhorenny....